La datation au carbone-14
Elle sert à dater des objets jusqu’à environ 50 000 ans. Elle est à ce titre assez souvent mise en doute par les partisans d’une terre jeune (6 ou 10 000 ans) sous le prétexte que l’on trouve du carbone 14 dans le pétrole ou le charbon. En effet, si le carbone 14 disparaît assez vite (voir plus bas),
Comment se fait-il que l’on en trouve dans du pétrole soi-disant vieux de millions d’années ?
Voyons cela.
Version courte :
même sous terre des réactions nucléaires fabriquent du C14.
Version (pas trop) longue ci-dessous.
Le carbone-14 est instable. Si j’en ai 8 000 exemplaires devant moi et que je vais me promener 5 700 ans, il n’en restera que 4 000 à mon retour. Une autre promenade de 5 700 ans, et il n’en restera que 2 000. Encore 5 700 ans, et il en restera 1 000. Etc. Tous les 5 700 ans c’est la même histoire : la quantité de C14 est divisée par 2. On dit que 5 700 ans, c’est la « demi-vie » du C14. En 1 million d’années, combien de fois mon stock de C14 sera-t-il donc divisé par 2 ? « 1 million divisé par 5 700 » fois, c’est-à-dire 174 fois. Et diviser 174 fois de suite par 2, c’est comme diviser par 2,4 x 1052, c’est-à-dire 24 suivi de 51 zéros. C’est beaucoup.
Comme le nombre d’atomes sur terre est d’environ 1 suivi de 50 zéros, on comprend que si notre planète était faite de C14 pur, elle aurait disparu en moins d’un million d’années.
La question se pose donc : si le pétrole a des millions d’années, comment se fait-il qu’on trouve du C14 dedans ? En effet, comme dirait Maire Folace des Tontons Flingueurs, « y’en a ». Mais d’où vient-il ?
Et dans l’atmosphère ?
On pourrait tout simplement commencer pas se demander comment il se fait que l’on trouve du C14 dans l’atmosphère puisque cette dernière a bien plus d’un million d’années.
C’est tout simplement que le C14 atmosphérique est renouvelé en permanence. Comme une baignoire qui fuirait, mais dont le robinet ne serait pas complétement fermé. Comment donc fait-on du C14 ?
La recette est assez simple et fait appel à de la physique nucléaire bien établie,
- Prenez le noyau d’un atome d’azote-14, 7 neutrons et 7 protons.
- Ajoutez-y un neutron[1] pour obtenir un azote-15, avec 8 neutrons et 7 protons.
- Attendez un peu (pas longtemps) et sans que vous n’ayez rien à faire, un proton est éjecté. Vous vous retrouvez ainsi avec un noyau qui contient 6 protons et 8 neutrons. C’est donc du carbone, à cause des 6 protons, et « 14 », car 6+8=14. Bref, du C14. On peut aussi finir avec un azote-15, mais c’est plus rare[2].
Bref, tout ce qu’il faut, c’est de l’azote-14 et un neutron[3]. Des neutrons, il y en pas mal qui se promènent dans l’atmosphère, et de l’azote, il y en a plein aussi. Aucun mystère donc à ce que l’on trouve du C14 là-haut. Ce qui s’y trouve diminue de moitié tous les 5 700 ans, mais on en fabrique en permanence. Au final, environ 1 atome de carbone atmosphérique sur 1 000 milliards est un C14. Le reste est presque exclusivement du C12, avec des miettes de C13.
Et en sous-sol ?
On y est presque. Pour faire du C14, il faut de l’azote et des neutrons. De l’azote, il y en a plein dans le pétrole.
Mais d’où viennent les neutrons ? De l’activité nucléaire de l’Uranium-238 et du Thorium-232 (la radioactivité est un phonème naturel. Faut pas le dire à Greenpeace). Ces deux-là sont présents sous terre, radioactifs, et quand ils se désintègrent, ce qu’ils font très lentement ayant des demi-vies énormes, ils expulsent un noyau d’hélium qui va générer des neutrons en tapant sur d’autres noyaux.
Bref, dessous, y’en a aussi. Des mesures du rapport C12/C14 ont donné des ratios environ 1 million de fois plus faible que dans l’atmosphère[4]. C’est pas beaucoup, mais y’en a. La science contemporaine se casse le nez sur bien des problèmes, mais pas sur celui-ci. Personne n’aura le Nobel pour ça.
La physique nucléaire : un jeu d’échec géant
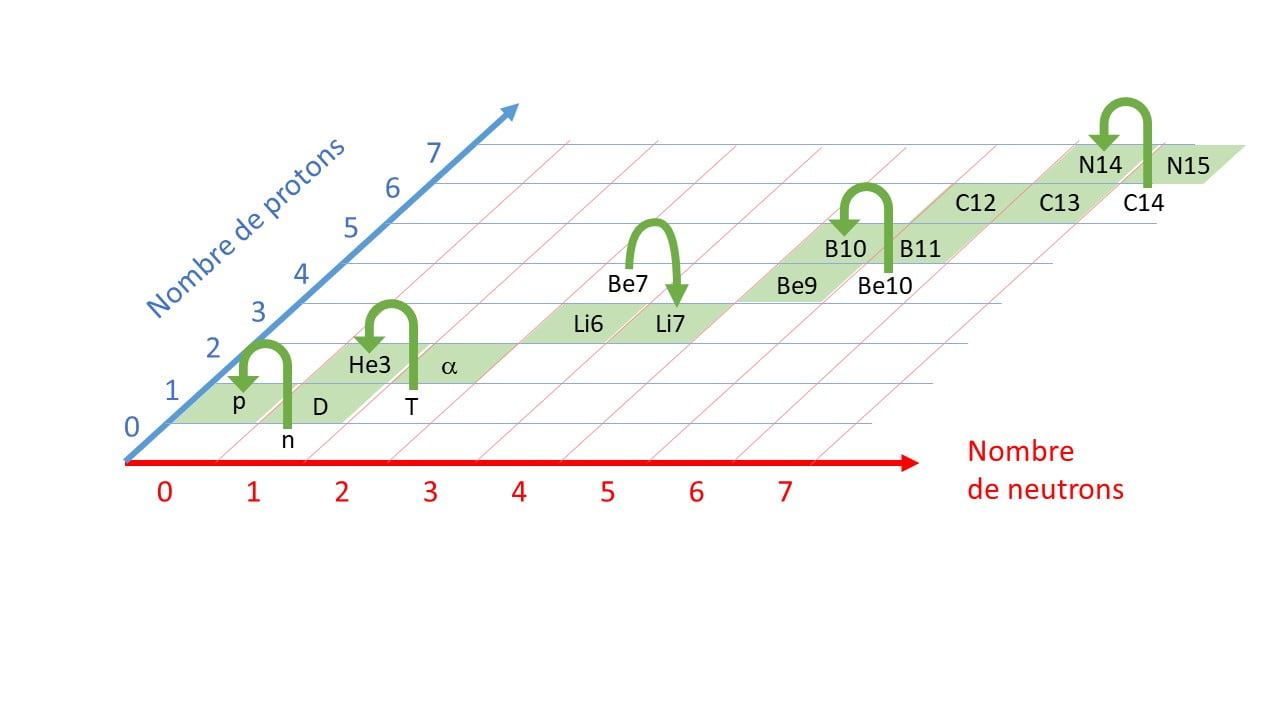
J’aimerais pour finir tenter de vous faire apprécier les richesses de la physique nucléaire. Le noyau d’un atome, ce sont des protons avec des neutrons. On peut donc représenter tous les noyaux sur une sorte de damier géant dont le commencement est dessiné ci-dessous. Chaque case est un noyau en puissance.
Pour des raisons que je ne préciserai pas, certaines cases sont vides. Vous n’arriverez pas à faire tenir ensemble 6 protons avec 1 neutron, par exemple. D’autres cases sont occupées par un noyau instable, comme le C14, le Be7 (Béryllium 7) ou le Be10. Les flèches indiquent où « saute » un noyau radioactif quand il se désintègre. En effet, « se désintégrer », pour un noyau, c’est se changer en un autre tout en expulsant quelque chose. Et si un noyau se change en un autre, cet autre est forcément sur le damier. Il n’y a pas d’autre endroit où aller. Finalement, d’autres cases sont occupées par un noyau stable, comme le D (Deutérium) ou bien le C12. Ce sont les cases vertes du diagramme.
Je n’ai représenté que la partie inférieure gauche du damier. On sait que l’axe des neutrons va jusqu’à 177 minimum. Et celui des protons, jusqu’à 118 au moins. On connait en tout plus de 3 000 noyaux dont 250 environ, seulement, sont stables[5]. Tous les autres sont radioactifs, avec des demi-vies qui vont du milliardième de seconde au millier de milliards d’années. Le lecteur intéressé par une vue d’ensemble du damier la trouvera ici, avec des infos détaillées sur chacun des 3 000 noyaux connus (il suffit de cliquer sur la case du damier). Quand on parle d’un travail de fourmis…
Quand on sait qu’un noyau peut sauter d’une case à l’autre, soit parce qu’il est instable (comme le C14 qui devient un N14), soit parce qu’il s’est pris dans la figure un neutron (comme le N14 qui devient un C14), on se rend compte que ce damier géant est le lieu d’une partie intense qui ne s’arrête jamais.
Une physique peu connue, d’une richesse exceptionnelle, et qui explique, entre autres, pourquoi on peut tout à fait trouver du C14 dans du pétrole enfoui depuis des millions d’années.
Pour aller plus loin
- Article en anglais détaillant ce que je viens de dire.
- Article Wikipedia sur la physique nucléaire.
- Pour avoir une idée des thèmes de recherches actuels dans le domaine : Physical Review C.
Notes
[1] Le neutron étant neutre, il rentre dans le noyau comme dans du beurre.
[2] Pour les geeks : la courbe ocre en descente sur ce graphique est la probabilité d’obtenir un C14 en fonction du neutron indicent. La rouge bordeaux, la plus basse, celle de finir avec un azote-15. Merci à Luc Bourhis pour le tuyau.
[3] On peut aussi partir d’un oxygene-17 ou d’une carbone-13, ou… de pas mal d’autres noyaux.
[4] Voir la première référence citée à la fin.
[5] Conclusion : sur 177 x 118 = 20 886 noyaux possibles, seuls 14% sont réalisables dans la nature et 1,2% sont stables.